کتاب اصول علم و مهندسی توسط قلم توانای استاد سید حسین تویسرکانی به تالیف درآمده و در دسترس علاقه مندان قرار گرفته است. هر مبحث این کتاب شما را به دریچهای از دانش علم مواد میبرد.در هر بخش میتوانید دانشی را کسب کنید که در دنیای به این بزرگی شاید کم کسی باشد که این اطلاعات را در اختیار داشته باشد.
امروز بخشی از کتاب اصول علم مهنرسی و مواد را با یکدیگر میخوانیم.
سختی
سختی به عنوان مقاومت یک ماده در مقابل تغییر شکل پلاستیکی و یا فرو رفتن ماده سختتر دیگری در آن تعریف شده است. سختی، یک خاصیت تعریف شده فیزیکی و استاندارد شده نیست، زیرا به وسیله عددی که از طریق یکی از روشهای به کار برده شده به دست میآید تعیین میشود. بسیاری از موارد آزمایش کشش، که از لحاظ تهیه نمونه وقتگیر و پر خرج است، توسط آزمایش ساده سختی جایگزین میشود. روشهای مختلفی برای تعیین سختی وجود دارد که هرکدام به نوبه خود مزایا و معایبی دارند و معمولا تمامی این روشها تا کنون در بررسیهای کنترل کیفی و کارهای تحقیقاتی بسیار سودمند بوده است.
گرمای ذوب و گرمای انجماد
در درجه حرارت صفر مطلق (۲۷۳- درجه سانتیگراد) اتمهای یک ماده کریستالی بیحرکت در محلهای شبکه خود قرار گرفتهاند و به اصطلاح یخ میزنند و با حرارت دادن به این ماده یخزده از خارج، اتمها در همان محل خود به ارتعاش در میآیند. هرچه درجه حرارت بالاتر رود، دامنه نوسان ارتعاش اتمها افزایش مییابد و در نتیجه انرژی داخلی آن با بالا رفتن درجه حرارت افزایش مییابد.
وقتی دما به حد معینی رسید، دامنه نوسان اتمها به قدری زیاد میشود که بر انرژی شبکه فائق آمده و شبکه به هم میریزد و بلور ذوب میشود. بنابراین عمل ذوب به علت ضعیف شدن یا شکسته شدن اتصالهایی است که یونها، اتمها و یا مولکولها را متصل به هم نگه میدارد. هر مادهای برای ذوب شدن به مقدار معنی انرژی احتیاج دارد. این مقدار انرژی را “گرمای ذوب ” یا به عبارتی “گرمای نهان ذوب” مینامند.
حرارت دادن در درجه حرارتهای بالا (نزدیک به نقطه ذوب) نه تنها باعث به وجود آمدن ارتعاشات حرارتی میشود، بلکه تعداد زیادی جای خالی تولید میکند. وقتی جاهای خالی – در یک ساختار کریستالی متراکم – به حدی رسید که باعث به هم خوردن عدد هماهنگی شد، در نتیجه نظم آرایشی اتمی از بین میرود و یک بینظمی یا آشوب در آن به وجود میآید.
از آنجا که گرمای ذوب، انرژی لازم برای ایجاد بینظمی در یک مُل از اتمهای ماده است، درجه حرارت ذوب مقیاسی برای اندازهگیری استحکام پیوند اتمی است.
برعکس در موقع تبدیل حالت مایع به جامد یعنی در هنگام انجماد، مقداری گرما یا به عبارتی انرژی حرارتی آزاد خواهد شد. این مقدار انرژی آزاد شده که به عنوان “گرمای انجماد” یا “گرمای تبلور” (گرمای کریستالیزاسیون) نامیده میشود، برابر گرمای ذوب است.
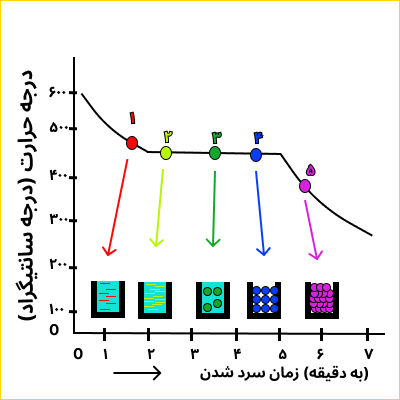
برای مثال انجماد سرب را در نظر میگیریم: انجماد سرب به طور ناگهانی انجام نمیگیرد، بلکه نسبت به مقدار مذاب و شرایط خارجی سرد شدن کم و بیش به مدت زمانی نیاز دارد. در شکل زیر نمودار انجماد سرب به صورت شماتیک رسم شده است.
در نقطه (۱) تمامی سرب به حالت مذاب است زیرا که درجه حرارتش بالای ۳۲۷ درجه سانتیگراد (نقطه انجماد) قرار دارد. به محض اینکه درجه حرارت مذاب به دمای انجماد رسید (نقطه ۲) جوانه زنی داخل مذاب شروع میشود و جوانهها به مرور رشد میکنند و متناسب با شکل گیری و رشد جوانههای کریستالی گرمای انجماد ازاد میشود (گرمای تبلور) که از کاهش درجه حرارت جلوگیری میکند. با ادامه عمل انجماد از یک طرف کریستالهای به وجود آمده رشد میکند و از طرف دیگر کریستالهای جدید به وجود میآید و مرتب از مقدار مذاب کاهش یافته و به مقدار جامد افزوده میشود (نقاط ۳ و ۴)، و بالاخره تمام سرب منجمد خواهد شد و چون در داخل سرب دیگر حرارت اضافی آزاد نمیشود، درجه حرارت شروع به پایین آمدن میکند (نقطه ۵).
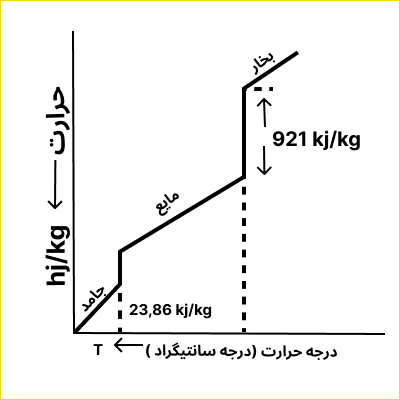
برعکس موقعی که سرب جامد حرارت داده میشود و به نقطه ذوب (۳۲۷ درجه سانتیگراد) برسد باید به سرب جامد گرمای ذوب به مقدار ۲۳/۹ j/g ph داده شود تا ایتکه تمامی سرب جامد به حالت مایع در آید مانند شکل پایین. به همین جهت است که در نمودار گرم کردن نسبت به زمان برای یک فلز خالص نقطه ذوب به صورت خط افقی (خط ثابت درجه حرارت) نمایان میشود.
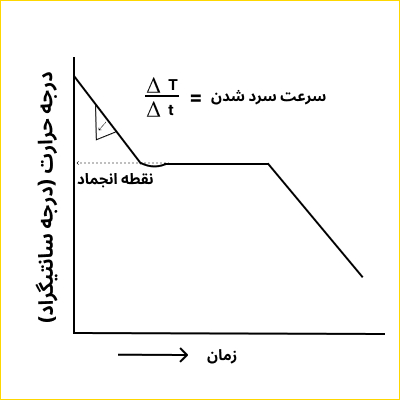
برای اینکه درجه حرارت ثابت نمودار سردن کردن نیز با دمای انجماد مطابقت کند لازم است که سرد کردن تا حد امکان به آرامی انجام گیرد، در غیر این صورت مذاب مقداری بیشترسرد میشود بدین ترتیب که متبلور شدن ابتدا در درجه حرارتهای پایینتر از نقطه ذوب شروع میشود، شکل زیر را مشاهده کنید.
موقعی که سرعت سرد کردن چندان زیاد نباشد، درجه حرارت مذاب مقداری پایینتر از نقطه انجماد آمده و مجددا هنگامی که گرمای انجماد آزاد میشود درجه حرارت بالا میرود. چنانچه سرعت سرد کردن بسیار زیاد باشد، گرمای آزاد شده به اندازهای نیست که بتواند مذابی را که زیادتر از نقطه انجماد (۳۲۷ درجه سانتیگراد) سرد شده مجددا به دمای انجماد برساند. در اینجا درجه حرارت ثابت در نمودار سرد کردن میتواند به طور قابل ملاحظهای از درجه حرارت حقیقی ذوب پایینتر باشد.
این پدیده میتواند همچنین در موقع سرد کردن بسیار آرام مذاب ظاهر شود و غالبا موقعی پیش میآید که ایجاد اولین جوانههای تبلور به عللی کند شود و یا مانعی برای به وجود آمدن آنها پیشآید که به وسیله هم زدن مذاب یا اضافه کردن کریستالهای بسیار کوچک از همان فلز (تقریبا معادل یک نوع تلقیح) میتوان از این نوع پایین آمدن درجه حرارت انجماد جلوگیری به عمل آورد.




نظری یافت نشد.